全程液体活检监测结直肠癌NeoRAS,抓住抗EGFR治疗机会
NeoRAS现象是指转移性结直肠癌(mCRC)经全身化疗后,肿瘤RAS状态由突变型(MT)转为野生型(WT)。西妥昔单抗是一种抗EGFR抗体,对RAS WT型mCRC患者有效,但对RAS MT型mCRC患者无效。然而,其在NeoRAS WT mCRC患者中的疗效尚不明确。本文报告了2例经抗EGFR治疗后有临床反应的NeoRAS WT mCRC患者。第1例是一名40岁男性,患同时性腹膜转移性直肠乙状结肠癌。对肿瘤组织的RAS检测显示KRAS G12C突变,根据液体活检的评估结果,该突变在二线化疗后转化为RAS WT。患者开始伊立替康联合西妥昔单抗治疗后,CT显示恶性腹水已消退。4个月后因疾病进展患者停止治疗。第2例为一名68岁男性患者,乙状结肠癌同时性肝转移。最初在肿瘤组织中检测到KRAS G12D突变,经6线化疗后液体活检未检出该突变。患者开始西妥昔单抗单药治疗后,肝转移灶明显缩小。患者继续西妥昔单抗单药治疗8个月,无疾病进展。本文的病例证明了抗EGFR治疗NeoRAS WT mCRC的疗效,并强调了在整个临床过程中监测基因突变谱对治疗选择的重要性。
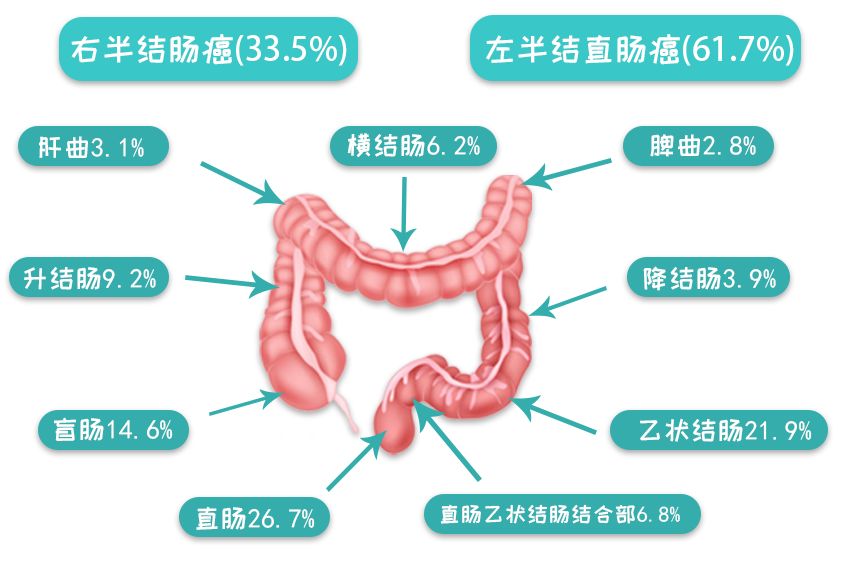
图片来源于网络,侵删
研究背景
转移性结直肠癌(mCRC)是全球癌症死亡的第二大原因。其预后仍然较差,但分子靶向药物的发展延长了mCRC患者的生存时间。目前,评估个体肿瘤的多基因变异并选择合适的分子靶向药物对于治疗mCRC至关重要。
约50%的mCRC患者存在RAS突变(KRAS或NRAS外显子2、3和4)。既往研究表明,抗EGFR抗体西妥昔单抗和帕尼单抗对RAS MT mCRC患者的生存获益低于RAS WT肿瘤患者。由于RAS突变是抗EGFR抗体疗效的负预测因素,因此国际实践指南建议mCRC患者在开始抗EGFR治疗之前进行RAS检测。此外,在3%的mCRC患者中发生的KRAS G12C突变已被确定不仅是抗EGFR抗体的负预测因素,而且是包括mCRC在内的实体瘤的新治疗靶点。
以前,RAS检测通常是对通过活检或手术获得的肿瘤组织进行。然而,这种肿瘤取样通常是有创的,难以重复。因此,在化疗期间监测RAS突变状态一直很困难。此外,利用肿瘤活检进行RAS检测的结果可能受到肿瘤空间异质性的限制。肿瘤异质性是指单个肿瘤由许多亚克隆细胞组成,使用一部分肿瘤组织进行的分析可能不能反映患者整个肿瘤的基因变异。
最近的研究表明,分析血液样本中的循环肿瘤DNA(ctDNA)是肿瘤活检的重要替代手段,可以检测突变和克服肿瘤的空间异质性。由于与常规组织取样相比,使用ctDNA的液体活检是一种无创方法,因此可以在整个临床过程中监测基因突变状态的变化。在之前的临床试验中,使用磁珠、乳剂、扩增和磁性数字聚合酶链反应(PCR;BEAMing)技术测定血浆ctDNA中的RAS突变状态与肿瘤组织DNA参考方法的一致性为86%-93%。
ctDNA液体活检技术的发展逐渐揭示了mCRC患者化疗过程中RAS基因突变状态的动态变化。有研究表明,在抗EGFR治疗过程中,部分mCRC患者的RAS基因突变状态由WT变为MT。RAS MT亚克隆的出现被很好地描述为在治疗诱导的选择压力下克隆演变的结果,从而导致抗EGFR治疗的获得性耐药。
另一方面,RAS MT逆转为WT被认为是罕见的,因为RAS MT克隆在肿瘤进化过程中具有预期的进化优势。然而,近年来研究发现,化疗过程中RAS MT逆转为RAS WT,即NeoRAS现象,越来越常见。NeoRAS现象的发生机制尚不明确,各报道发生率差异较大,范围为10.7%-83.3%。研究者有必要考虑NeoRAS WT mCRC患者可否像RAS WT mCRC患者一样从抗EGFR治疗中获益,因为与RAS WT mCRC患者相比,RAS MT mCRC患者的治疗选择有限。然而,很少有报道描述抗EGFR治疗NeoRAS WT型mCRC患者的临床疗效。本文报道了2例经抗EGFR治疗后获得临床反应的NeoRAS WT型mCRC,并进行了文献综述。
病例1:40岁男性直肠乙状结肠癌同步腹膜转移患者
一名40岁男性患者因便秘就诊,诊断为同时性腹膜转移的直肠乙状结肠癌(根据国际癌症控制联盟TNM第8版,T4aN2bM1c IVC期)。因直肠梗阻,急诊行腹腔镜辅助高位前切除术。病理检查显示原发肿瘤为高分化腺癌。使用PCR-rSSO方法对原发肿瘤组织进行突变分析,发现KRAS G12C突变,NRAS和BRAF WT。基于PCR方法检测微卫星不稳定性(MSI),结果为阴性。除了上述基因变异之外,使用OncoGuide?NCC Oncopanel系统对原发肿瘤组织进行的基因分析,发现了几个致癌基因变异。术后,患者开始接受卡培他滨、奥沙利铂和贝伐珠单抗(CapOX+BEV)作为一线全身化疗。根据实体瘤疗效评价标准1.1评估,部分缓解(PR)是肿瘤缓解。CapOX+BEV开始治疗15个月后,CT显示腹水增加,并提示疾病进展。随后,启动了氟尿嘧啶、亚叶酸、伊立替康和雷莫芦单抗(FOLFIRI+RAM)方案作为二线化疗,但1.5个月后因疾病进展停用了该方案。在每次一线和二线化疗结束时,使用基于BEAMing技术的 OncoBEAM? RAS CRC试剂盒进行液体活检。虽然此前原发肿瘤组织的突变检测发现KRAS G12C突变,但两次液体活检均未检测到RAS突变。在患者同意的情况下,开始将伊立替康联合西妥昔单抗作为三线化疗。2个月后,CT扫描显示腹水消失。治疗期间无严重不良事件发生。西妥昔单抗治疗4个月后,腹膜转移进展。随后开始使用曲氟尿苷/替吡嘧啶(FTD/TPI)+BEV和瑞戈非尼治疗,均疾病进展。该患者目前正在接受好的支持性治疗。
病例2:68岁男性乙状结肠癌同步肝转移患者
1例68岁男性患者被诊断为乙状结肠癌伴肝脏及淋巴结多发转移(根据国际癌症控制联盟TNM第8版,T3N2bM1b IVB期)。原发肿瘤病理诊断为高分化腺癌。对原发肿瘤组织进行突变分析,发现KRAS G12D突变、NRAS和BRAF WT。使用基于PCR的方法进行MSI检测,结果为阴性(非MSI-H)。切除原发肿瘤后,患者接受了6线全身化疗:FOLFOX(氟尿嘧啶、亚叶酸钙、奥沙利铂)+BEV、FOLFIRI+BEV、FTD/TPI+BEV、瑞戈非尼、再次FOLFOX+BEV,以及试验性免疫治疗。一线应用FOLFOX+BEV方案化疗,肿瘤反应为PR。然而,其他治疗方案未能使肿瘤缩小,并且均以疾病进展告终。在FOLFOX+BEV再次治疗期间,使用Foundation One Liquid CDx?Assay 进行了全面的基因组分析。结果显示有几个可干预的基因变异和高肿瘤突变负荷,但未发现KRAS G12D突变。试验性免疫治疗完成后,使用 OncoBEAM? RAS CRC试剂盒重新评估了KRAS突变状态,结果显示RAS为WT,在患者同意的情况下,西妥昔单抗单药治疗开始作为七线治疗。3个月后,CT扫描显示肝转移灶明显缩小。患者继续西妥昔单抗单药治疗8个月,无疾病进展。治疗期间未观察到严重不良事件。然而,患者在西妥昔单抗治疗10个月后死于癌症进展。
讨 论
抗EGFR抗体在NeoRAS WT型mCRC中的应用仍有争议,但由于RAS MT型mCRC的治疗方案有限,因此值得研究。之前的几项研究提示,抗EGFR抗体对NeoRAS WT mCRC有效。然而,所有这些结果均是在联合细胞毒性化疗的情况下获得,抗EGFR抗体在多大程度上促成了这些结果尚不清楚。在病例2中,西妥昔单抗单药治疗开始后,观察到肿瘤缩小。本报告显示了抗EGFR抗体单药治疗NeoRAS WT mCRC的疗效。本研究更明确地提示,抗EGFR抗体有效,至少对部分NeoRAS WT型mCRC患者有效。评估抗EGFR抗体治疗NeoRAS WT mCRC疗效的几项前瞻性临床试验目前正在进行中。
本组病例不同时间的RAS基因突变检测结果存在差异。所有的检测都是根据说明书进行的,因此研究者不认为差异是由检测技术引起的。虽然这种NeoRAS现象的机制尚不清楚,但可能与肿瘤内异质性和化疗诱导的克隆演变有关。也就是说,全身化疗在消除最初优势的RAS MT亚克隆的同时,增加了次要克隆——RAS WT亚克隆的比例,从而导致了NeoRAS现象。事实上,Klein-Scory等证明,在对化疗有应答的RAS MT mCRC患者中,超过90%的患者的RAS MT克隆在化疗期间迅速消失,并转化为RAS WT克隆。较长的RAS检测间隔,以及第二次采样前对化疗的良好反应,与NeoRAS现象相关,提示化疗引起的克隆演变导致了NeoRAS现象。从这个角度来看,RAS MT亚克隆可能存在于低于ctDNA检测下限的NeoRAS WT肿瘤患者的血浆样本中。然而,即使是这样,也不能否定抗EGFR治疗NeoRAS WT型mCRC的疗效,因为已有研究表明,RAS低突变丰度(0.1-5%)的患者可能从化疗加用西妥昔单抗中获益。根据实体瘤疗效评价标准,这2例患者在一线化疗期间均达到了PR, RAS检测的采样间隔为15个月。其临床过程支持化疗诱导的克隆演变和NeoRAS现象之间存在关联。在未来的研究中,使用基线或来自多个病变的肿瘤组织的ctDNA进行深度测序的基因突变分析可能有助于阐明肿瘤内异质性和克隆进化在NeoRAS现象中的作用。
本文的两个病例强调了在整个治疗过程中重复进行基因分析和实时了解mCRC患者基因突变谱的重要性。病例1在化疗诱导前肿瘤组织样本中检测到KRAS G12C突变,KRAS G12C抑制剂的疗效值得期待。然而,一线化疗后的液体活检显示肿瘤的RAS状态已转变为NeoRAS WT。虽然KRAS G12C抑制剂对NeoRAS WT mCRC的疗效尚不明确,但考虑到NeoRAS现象,治疗前的RAS检测可能是KRAS G12C抑制剂适应证的理想选择。病例2在西妥昔单抗治疗前进行了全面的基因分析,未发现RAS MT、HER2扩增或BRAF V600E MT等预测抗EGFR抗体疗效的负因子。该病例表明,全面的基因突变分析可能能够有效预测哪些患者将从高效的抗EGFR抗体中获益。
本文展示了两例在组织和血液样本检测中存在RAS基因状态差异的mCRC病例。2例患者最初均通过原发肿瘤组织诊断为RAS MT mCRC,但全身化疗后的液体活检显示为RAS WT状态。这些NeoRAS WT mCRC患者对抗EGFR治疗有临床反应。虽然NeoRAS现象的病因和临床意义尚不完全清楚,但已有研究表明,抗EGFR抗体对部分NeoRAS WT型mCRC患者有效。此外,本文病例强调了在整个临床过程中(而不是仅仅一次)监测基因突变谱对选择治疗方案的重要性。
文章摘自网络,侵删
同类文章排行
- 这款EGFR靶向药「换个用法」就能破解「肺控脑不控」难题?控制率100%,中位PFS已超20个月!
- 8月重磅!药监局批准3款NK细胞,为肝癌、胃癌、肺癌等带来生命火种,最长无病生存近4年
- 在肝癌治疗中添加细胞疫苗可减缓癌症进展,病情无进展生存时间大幅度提升80%!
- 质子与光子全脑全脊髓照射治疗软脑膜病变的真实世界经验
- 年轻人胃癌发病率30年翻一番
- 聚焦生存差异|HER2阳性晚期乳腺癌患者短期与长期生存的相关因素分析
- 女演员片场呕血确诊癌症!本人崩溃发声
- 柳叶刀惊曝:AI让医生“自废武功” 癌症检出率崩盘
- 全球首个HER2突变晚期非小细胞肺癌口服靶向药圣赫途在华获批
- 宗艾替尼在华获批,用于非小细胞肺癌治疗
最新资讯文章
您的浏览历史