Nature:揭示产热脂肪细胞的交感神经支配机制,有望开发出新的抗肥胖策略
交感神经系统通过从局部轴突释放去甲肾上腺素来驱动棕色脂肪细胞(brown adipocyte)和米色脂肪细胞(beige adipocyte)产热。然而,与白色脂肪组织相比,较高水平的产热脂肪组织的交感神经支配的分子基础仍然未知。
在一项新的研究中,来自美国达纳法伯癌症研究所和哈佛医学院的研究人员发现产热脂肪细胞表达一种之前未知的哺乳动物特异性的内质网蛋白,他们称之为Calsyntenin 3β(CLSTN3β)。相关研究结果发表在2019年5月9日的Nature期刊上,论文标题为“Innervation of thermogenic adipose tissue via a calsyntenin 3β–S100b axis”。
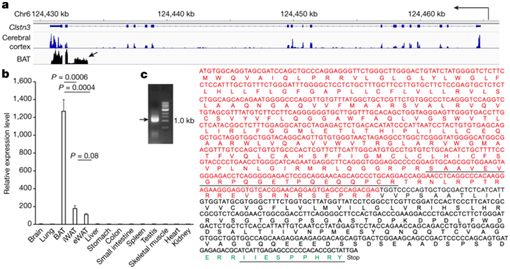
图片来自Nature, 2019, doi:10.1038/s41586-019-1156-9。
脂肪细胞中的Calsyntenin 3β表达的缺失或获得分别减少或增强脂肪组织中的功能性交感神经支配。剔除Calsyntenin3β使得摄入高脂肪饮食的小鼠易变得肥胖。从机制上说,Calsyntenin 3β促进来自棕色脂肪细胞的蛋白S100b---一种缺乏信号肽的蛋白---的内质网定位和分泌。S100b在体外刺激交感神经元的神经突向外生长。S100b缺乏在表型上类似于Calsyntenin 3β缺乏,并且在棕色脂肪细胞中强迫表达S100b可拯救由Calsyntenin3β剔除引起的缺陷性交感神经支配。
由上可知,这些研究结果揭示出产热脂肪细胞和交感神经元之间存在一种哺乳动物特异性的通讯机制。
文章来源网络,如有侵权,请联系删除。
同类文章排行
- 管好这三步,RET融合肺癌患者少走弯路,活得更长更好!
- EGFR突变患者进展了别慌,从耐药检测到治疗选择这样做能找到新出路
- 这种药会降低10倍生存期,请肺癌患者警惕使用!
- 免疫治疗对EGFR突变肺癌有效吗?
- 新型免疫细胞疗法TILS,仅一次治疗为晚期头颈癌患者带来“稳定”的希望!
- 晚期肺癌跨过9年!他坦白秘密:抗癌4大法宝里,这件事最有效
- 演员李菁菁瘦到认不出 曾患乳腺癌如今已战胜病魔
- 临床植入式电极精准定位脑深部肿瘤边界
- 当FDA超级加倍重视OS,能否影响肿瘤药物研发格局?
- 预后极差、治疗选择有限 HER2突变晚期非小细胞肺癌患者迎创新疗法
最新资讯文章
您的浏览历史