鉴定出癌细胞逃避铁死亡新机制
化疗通过阻止癌细胞增殖并诱导“细胞死亡”来杀死它们。细胞死亡的一种形式称为铁死亡(ferroptosis)---铁依赖性细胞死亡---是由构成细胞膜的脂肪(脂质)降解引起的。很多侵袭性和抗药性的癌症易受铁死亡的影响,但是在一项新的研究中,来自德国维尔茨堡大学和亥姆霍兹慕尼黑中心等研究机构的研究人员发现了一种让癌细胞对铁死亡产生抵抗力的新机制。这就为开发抑制这种新发现机制从而允许铁死亡在易感的癌细胞中发生的药物提供了一种新的靶标。相关研究结果于2019年10月21日在线发表在Nature期刊上,论文标题为“FSP1 is a glutathione-independent ferroptosis suppressor”。
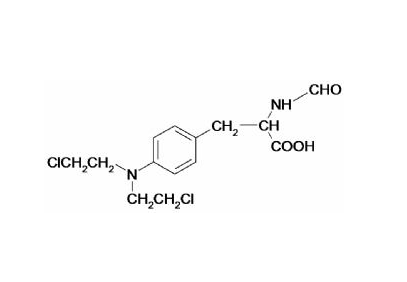
图片来自Nature, 2019, doi:10.1038/s41586-019-1707-0。
论文共同作者、英国帝国理工学院化学系的Edward Tate教授说,“发现细胞获得抗药性的全新方式将使得我们能够设计靶向这种机制的药物。事实上,我们已经有了我们之前开发的间接地靶向这种机制的先导药物,并且正在实验室测试它们。”
铁死亡依赖于细胞膜上脂质的氧化---让这些脂质失去电子,从而导致它们降解。众所周知,一种称为谷胱甘肽过氧化物酶4(GPX4)的分子可以逆转这一过程,因而起着脂质抗氧化剂的作用。有一些靶向GPX4的药物,但是大多数癌症仍然对铁死亡有抵抗力。
如今,这些研究人员发现另一种称为FSP1的分子,该分子也起着脂质抗氧化剂的作用,即便癌细胞缺乏GPX4,它也可将它们从铁死亡中拯救出来。除了确定FSP1在阻止铁死亡中的作用外,他们还发现几种潜在的使用药物靶向它的方法,因而降低对铁死亡产生的抵抗力。
为了发挥作用,FSP1需要一种称为N-肉豆蔻酰基转移酶(N-myristoyltransferase, NMT)的酶的帮助。在此之前,帝国理工学院的Tate及其团队开发出抑制NMT活性以便阻止普通感冒病毒感染的先导药物。
论文共同作者、帝国理工学院化学系Tate团队的博士生Andrea Goya Grocin使用了帝国理工学院开发出的一系列化学工具来研究FSP1和NMT对它的修饰。Andrea说,“由于抗药性肿瘤对铁死亡产生抵抗力,基于抑制FSP1、GPX4、NMT或者其组合来开发促进铁死亡的治疗方法有很大的潜力转化为未来的临床应用。”
文章来源网络,如有侵权,请联系删除。
同类文章排行
- 广泛期小细胞肺癌二线治疗新进展:安罗替尼+伊立替康,能带来哪些新希望?
- 全球首个针对DLL3的三特异性抗体与创新双抗药联合治疗小细胞肺癌,获批临床试验
- 奥希替尼耐药后怎么办?EGFR突变非小细胞肺癌患者的“第二战场”:埃万妥单抗?
- 肺癌没法手术?神药DS-8201+免疫治疗“逆转困局”真实案例!9个月无复发!
- 近40%胃癌患者的新希望!Satri-cel首次让CAR-T治疗实体瘤取得“硬胜利”
- 免疫治疗正在改变癌症治疗,但高血糖风险需要警惕
- EBC-129:靶向CEACAM5/6的新型ADC,为胰腺癌治疗打开新局面!
- 免疫治疗必读:下午3点前用药效果最佳!无进展生存期翻倍!
- 面对奥希替尼耐药,Necitumumab的加入能否逆转局面?
- HER2突变型晚期非小细胞肺癌脑转移的生存及预后因素
最新资讯文章
您的浏览历史